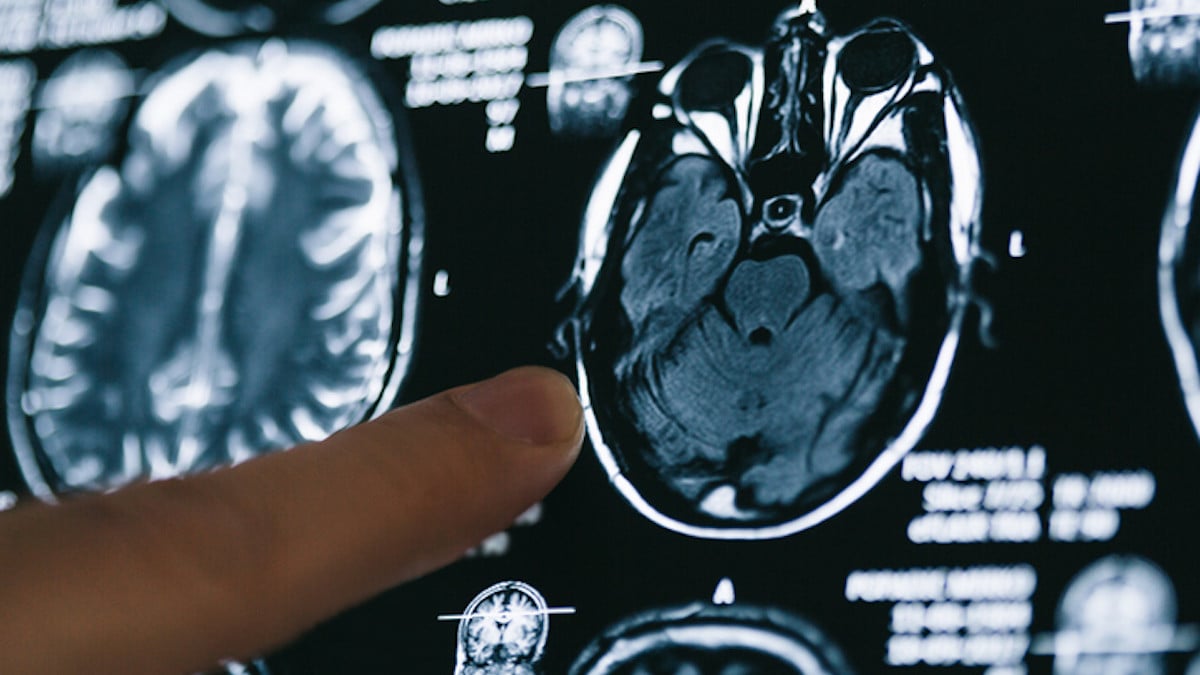
Des scientifiques de l’université de Barcelone ont découvert que la médecine s’acharnait sur le mauvais coupable, depuis des décennies, dans la recherche contre la maladie d’Alzheimer.
Depuis des décennies, la recherche contre la maladie d’Alzheimer se concentre sur une seule et même cible : les fameuses plaques amyloïdes qui étouffent peu à peu nos neurones.
Pourtant, malgré des milliards d’investissements, les traitements actuels ne parviennent qu’à freiner timidement ce naufrage tragique. Aujourd’hui, des biologistes de l’Université de Barcelone viennent de renverser totalement la table, en publiant les résultats de leur étude dans la revue Molecular Therapy.
En partant du principe que nous nous attaquions aux conséquences plutôt qu’à la racine du mal, ils ont développé un composé inédit capable de « reprogrammer » directement la machinerie génétique de notre cerveau. Une avancée spectaculaire qui ne se contente plus de ralentir la démence, mais qui commence déjà à en effacer les dégâts en laboratoire.
 Crédit photo : iStock
Crédit photo : iStock
Jusqu’à présent, l’arsenal médical reposait sur des anticorps monoclonaux (comme le lecanemab ou le donanemab) conçus pour faire le ménage dans le cerveau en détruisant les amas de protéines bêta-amyloïdes et tau. Si ces médicaments représentent une véritable prouesse technique, leur efficacité clinique reste plafonnée. Administrés très tôt, ils ralentissent le déclin cognitif d’environ 30 %.
C’est une victoire partielle, mais l’incapacité de ces traitements à restaurer la mémoire perdue a poussé les chercheurs à une remise en question vertigineuse : et si ces fameuses plaques n’étaient que les cicatrices de la maladie, et non son véritable moteur ?
C’est ici qu’intervient le composé FLAV-27, une molécule qui change radicalement de champ de bataille. Au lieu de nettoyer les protéines toxiques, ce traitement s’attaque à l’épigénome humain. Pour faire simple, il s’agit du système d’interrupteurs moléculaires qui décide d’activer ou d’éteindre nos gènes.
 Crédit photo : iStock
Crédit photo : iStock
Un composé qui bloque l'enzyme responsable de la maladie d'Alzheimer
Dans le cas de la maladie d’Alzheimer, une enzyme spécifique appelée G9a s’emballe et commence à « réduire au silence » des gènes absolument vitaux pour la plasticité de nos synapses et le traitement de nos souvenirs.
Le composé FLAV-27 agit comme un brouilleur extrêmement précis : il bloque chimiquement cette enzyme défaillante. Privée de son carburant, l’enzyme G9a lâche prise, permettant aux gènes de la mémoire de s’exprimer à nouveau normalement.
Les résultats publiés dépassent les attentes de l’équipe scientifique. Lors des tests effectués sur des nématodes (de petits vers de laboratoire), le FLAV-27 a non seulement prolongé leur durée de vie, mais a également boosté la respiration de leurs cellules et amélioré leur mobilité.
 Crédit photo : iStock
Crédit photo : iStock
Le succès s’est confirmé sur des modèles de souris atteintes de formes précoces et tardives d’Alzheimer. En calmant ce dérèglement génétique, le composé a réussi un exploit inédit : il a restauré les performances de la mémoire spatiale, relancé les comportements sociaux des rongeurs et réparé les connexions synaptiques endommagées. Cerise sur le gâteau, cette reprogrammation a naturellement entraîné une diminution des plaques amyloïdes, prouvant que ces dernières sont bien un symptôme secondaire d’un chaos génétique plus profond.
Si ce renversement de la maladie est une lueur d’espoir immense pour des millions de familles, la prudence reste de mise. Le FLAV-27 doit encore franchir la redoutable étape des essais cliniques sur l’Homme.
Avant qu’un tel médicament ne vous soit prescrit, l’équipe va devoir mener des études toxicologiques approfondies sur au moins deux espèces animales distinctes pour s’assurer que cette reprogrammation épigénétique est sans danger à long terme. Quoi qu’il en soit, la science vient de prouver que la démence n’est peut-être pas une fatalité irréversible, mais une simple erreur de codage que nous sommes enfin en train d’apprendre à corriger.