Dans une étude publiée dans la revue PNAS Nexus le 18 février dernier, des scientifiques japonais ont révélé avoir réussi à supprimer in vitro le chromosome responsable de la trisomie 21.
Voici une avancée qui pourrait révolutionner la médecine concernant la trisomie 21. Des scientifiques japonais, dirigés par le Dr. Ryotaro Hashizume, ont réalisé un exploit révolutionnaire en utilisant CRISPR pour éliminer le chromosome 21 supplémentaire qui cause le syndrome de Down, restaurant la fonction cellulaire normale.
L’outil CRISPR-Cas 9, dont la découverte a été distinguée par un prix Nobel en 2020, est un outil de modification du génome. Il est plus facile et plus rapide à utiliser que les techniques antérieures, une approche prometteuse pour la thérapie génique, qui vient de prouver une nouvelle fois son efficacité en supprimant le 3e chromosome 21.
Affectant 1 naissance sur 700 dans le monde, la trisomie 21 résulte d’une copie supplémentaire du chromosome 21, entraînant des déficiences intellectuelles, des caractéristiques distinctives et des problèmes de santé comme des malformations cardiaques et la maladie d’Alzheimer à début précoce.
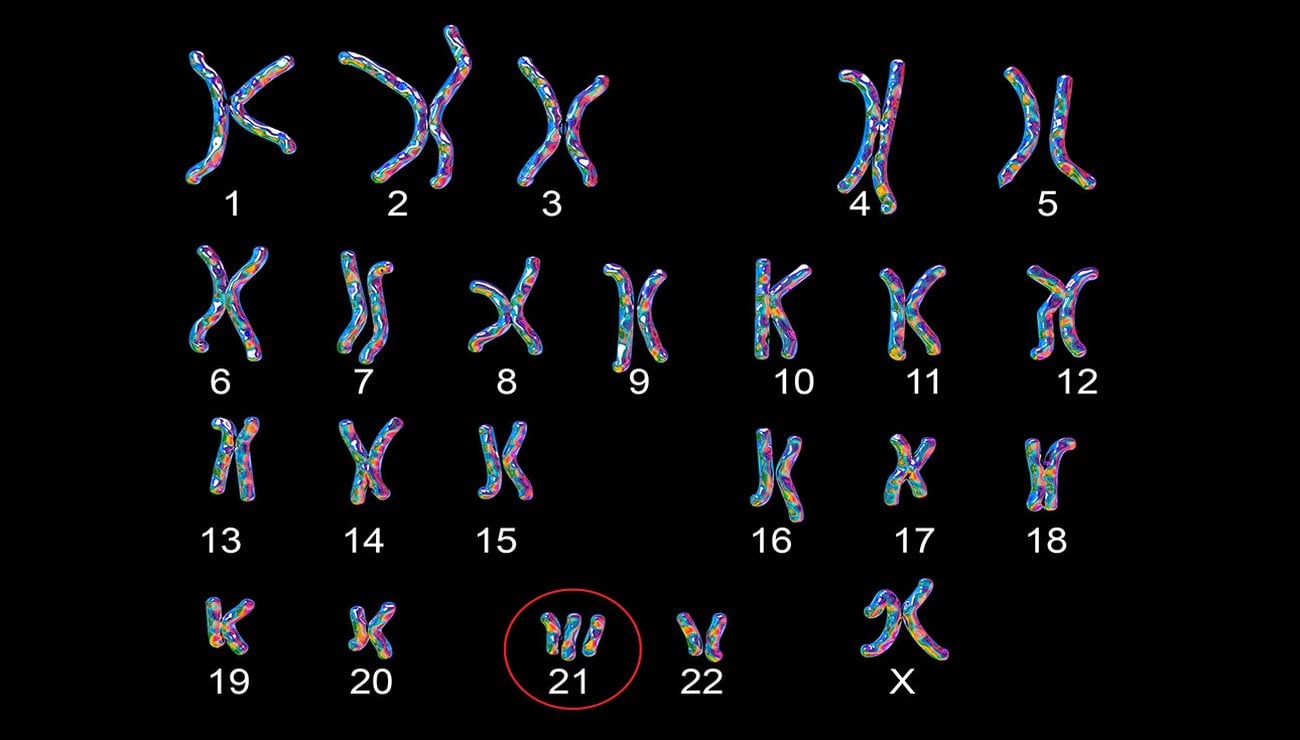 Crédit photo : D.R.
Crédit photo : D.R.
La technique de précision d’édition génétique de l’équipe, « édition spécifique aux allèles », entraîne CRISPR-Cas9 à cibler des séquences uniques sur le chromosome supplémentaire, en le coupant pour le déstabiliser et le rejetant naturellement lors de la division cellulaire, laissant ainsi la paire normale intacte.
Une prouesse à nuancer
L’étude a atteint un succès de 30,6 % dans l’élimination du chromosome supplémentaire, avec des cellules traitées (à la fois les cellules souches et les cellules de peau mature des patients atteints de trisomie 21) montrant une expression génique normalisée, la production de protéines et les taux de survie.
 Crédit photo : iStock
Crédit photo : iStock
C’est la première fois que la cause profonde a été abordée au niveau cellulaire, offrant un espoir sans précédent.
Cependant, le scepticisme demeure : l’efficacité de 30,6 %, bien que prometteuse, est loin d’être universelle, et les modifications hors cible ou les risques de mosaïcisme (où certaines cellules conservent le chromosome supplémentaire) doivent être examinées.
Les applications cliniques sont attendues dans des années, nécessitant des essais de sécurité approfondis, et des préoccupations éthiques concernant la modification de la lignée germinale persistent.






